多くのがん細胞は、「不死化スイッチ」をはじくと、無限に分裂する可能性があります。これは、他のほとんどの種類の細胞では実行できないトリックです。現在、研究者たちはこのスイッチを短絡させる方法を発見しました。これにより、ジョンマケイン上院議員が先月から亡くなった種類の脳腫瘍など、50種類以上の癌の広がりを遅らせたり、止めたりすることができます。
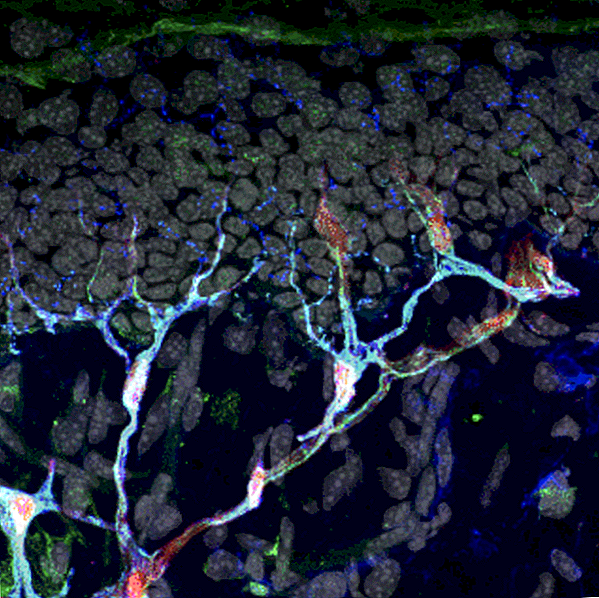
新しい研究では、研究者らは、がん患者から取り除かれた神経膠芽腫の脳がん細胞を調査し、GABPと呼ばれる一般的なタンパク質の小さなセグメントが、がん細胞がいわゆる不死スイッチを活性化できるようにするための鍵であることを発見しました。研究者がそのタンパク質セグメントを取り除いたとき、癌細胞は-実験皿とマウスの両方に移植されて-貪欲な増殖を停止し、単なる死の細胞のように振る舞った。
脳神経外科の教授であり、カリフォルニア大学サンフランシスコ校の神経腫瘍学の専門家であるジョセフコステッロが率いる研究者たちは、GABPのごく一部を阻害し、がん細胞から主要な細胞を奪う薬を開発することを望んでいると語った。他のセルへの悪影響を回避しながらスイッチに。 (Costelloは、彼と共同執筆者が製薬会社GlaxoSmithKlineと提携して医薬品としての可能性のある小分子を探索しているTelo Therapeuticsの創設者であることを研究で明らかにしました。)
調査結果は、本日(9月10日)、Cancer Cell誌に掲載されました。
未チェックの部門
癌細胞の特徴は、チェックされずに分裂する能力です。他のほとんどすべての細胞は、死ぬまでに設定された回数だけ分裂できます。主な例外は幹細胞です。幹細胞は、生物の生涯を通じて分裂して、血液や皮膚細胞など、死んでいる他のすべての細胞を補充することができます。
細胞の寿命は、テロメアと呼ばれる構造によって設定されます。テロメアは、染色体の両端を覆い、靴ひものアグレットのように機能します。各細胞分裂で、テロメアは少し短くなり、最終的にはテロメアが短すぎて染色体の完全性を保護できなくなります。それが細胞分裂が止まる時です。
幹細胞は、テロメアを再構築する酵素であるテロメラーゼを使用することにより、この死亡率から脱出します。間接的な方法で、テロメラーゼ逆転写酵素の略であるTERTと呼ばれる遺伝子の変異を利用することにより、多くの癌細胞はほとんど同じことを行います。この遺伝子のスイッチを入れることができる癌細胞は、幹細胞のように、無期限に分裂することができます。
科学者たちは、がんが不死のスイッチを何年も使用していることを理解してきました。以前の研究では、腫瘍の90%以上に突然変異があり、その増殖によりTERT発現がオンになり、テロメラーゼが産生されることがわかりました。しかし、テロメラーゼをブロックするだけの抗がん剤は、患者にとって毒性が高すぎることが証明されています。これは、薬も幹細胞を詰まらせ、新しい血液細胞や他の重要な細胞を生成する患者の能力を制限するためです。
Costelloのグループは、最も侵襲性の高い脳癌である膠芽腫に焦点を当て、幹細胞を使わずに、癌細胞のみの不死化スイッチへのアクセスを制限する方法を発見しました。具体的には、がん細胞がGABPbeta1Lと呼ばれるGABPタンパク質の一部を使用してスイッチをアクティブにしていることを発見しました。
GABPタンパク質は多くの種類の細胞でさまざまな作業に使用されているため、このタンパク質を完全に阻害すると、全身に悪影響が及ぶ可能性があります。研究者たちは、代わりに遺伝子編集ツールCRISPRを使用してGABPbeta1L要素のみを削除する実験を行いました。
そしてそれはうまくいった。研究者が実験室の皿やマウスで行った実験によると、beta1Lを欠くGABPタンパク質は癌細胞に有害な影響を及ぼしたが、他の細胞には影響を与えなかった
「これらの調査結果は、beta1Lサブユニットが積極的な神経膠芽腫および潜在的にTERTプロモーター変異を伴う他の多くの癌の有望な新薬標的であることを示唆している」とCostelloは記者発表で述べた。
膠芽腫の標的?
マケインとジョー・バイデン前副大統領の息子ボー・バイデンの両方が膠芽腫で死亡した。膠芽腫の形態にTERTプロモーター変異があったかどうかは公には知られていないが、推定83パーセントの膠芽腫がそのような変異を持っていることを考えると、コステロはLive Scienceにその可能性があると語った。
ボルティモアにあるジョンズホプキンスシドニーキンメル総合がんセンターの脳がんプログラムの共同リーダーであるジョンラテラ博士は、この研究には参加していなかったが、この調査結果は「運転におけるTERTの既知の役割を考えると、潜在的な重要性が高いと述べた。癌細胞の不死と神経膠腫の悪性腫瘍。
「この調査結果は、GABPbeta1Lやその他のレギュレーターの阻害を特定することに向けられた将来の研究に説得力のある議論を提供します」不死化スイッチをアクティブにするGAPBの能力は、LaterraにLive Scienceに語った。
彼は、この実験を他の腫瘍モデル、できれば患者のサンプルに直接由来するもので再現することが重要だと付け加えた。また、GABPbeta1Lが不足しているがん細胞は、マウスへの移植後にあまり積極的に成長しなかったが、マウスでのより多くの作業が必要であるとラテラは述べた。研究者は、マウスですでに発生した癌がGABPbeta1Lをブロックまたは除去することによって停止できるかどうかを決定する実験を計画する必要があると彼は言った。
Costello氏は、彼のグループと他の共同研究者は、GABPbeta1Lを標的とする小分子薬の作成と、GABPbeta1Lを生成しないようにヒトの遺伝子を変化させることができるCRISPRベースの治療法の開発を並行して進めると語った。この実験では、マウスに移植されたヒト脳癌細胞に対してCRISPRアプローチが行われました。研究者たちは前のプロジェクトでGSKと協力しています。ただし、どちらのアプローチも非常に実験的であり、開発には数年かかると、コステロはLive Scienceに語った。