20世紀初頭は、科学にとって非常に縁起の良い時期でした。アーネスト・ラザフォードとニールス・ボーアが素粒子物理学の標準モデルを生み出したことに加えて、それは量子力学の分野でのブレークスルーの時代でもありました。電子の振る舞いに関する継続的な研究のおかげで、科学者たちはこれらの素粒子が古典的なニュートン物理学に反する方法で振る舞う理論を提案し始めました。
そのような例の1つは、Erwin Schrodingerによって提案された電子雲モデルです。このモデルのおかげで、電子は、固定軌道で中心核の周りを移動する粒子として描かれなくなりました。代わりに、シュレディンガーは、科学者が電子の位置に関して知識に基づいた推測しかできないモデルを提案しました。したがって、それらの位置は、電子が検出される可能性が高い核の周りの「雲」の一部であるとしか記述できません。
20世紀への原子物理学:
原子理論の最も初期の既知の例は、古代ギリシャとインドに由来します。デモクリトスなどの哲学者は、すべての物質は、小さく分割不可能な単位で構成されていると仮定しました。 「原子」という用語は古代ギリシャで作られたものであり、「原子論」として知られる学派を生み出しました。しかし、この理論は科学的なものというよりも哲学的な概念でした。
原子の理論が科学的な問題として明確になり、証拠に基づく最初の実験が行われたのは、19世紀まででした。たとえば、1800年代初頭、イギリスの科学者であるジョンダルトンは、原子の概念を使用して、化学元素が特定の観察可能な予測可能な方法で反応する理由を説明しました。ガスに関する一連の実験を通じて、ダルトンはダルトンの原子理論として知られているものを発展させました。
この理論は、質量と明確な比率の会話の法則を拡張し、5つの前提に達しました。最も純粋な状態の要素は、原子と呼ばれる粒子で構成されます。特定の元素の原子は、最後の原子まですべて同じです。異なる元素の原子は、その原子量によって区別できます。元素の原子が合体して化合物を形成する;原子は化学反応で作成したり破壊したりすることはできず、グループのみが変化します。
電子の発見:
19世紀後半までに、科学者たちはまた、原子は複数の基本単位で構成されていると理論化し始めました。しかし、ほとんどの科学者は、この単位が最小の既知の原子-水素のサイズであると冒険しました。 19世紀の終わりまでには、ジョセフジョントムソン卿などの科学者によって行われた研究のおかげで、彼は劇的に変化するでしょう。
トムソンは、陰極線管(Crookes ’Tubeとして知られています)を使用した一連の実験を通じて、電界と磁場によって陰極線が偏向する可能性があることを観察しました。彼は、光で構成されるのではなく、水素よりも1000倍小さく、1800倍軽い負に帯電した粒子で構成されていると結論付けました。

これは、水素原子が物質の最小単位であるという考えを事実上反証し、トンプソンはさらに、原子が分割可能であると示唆した。正と負の両方の電荷で構成される原子の全体的な電荷を説明するために、トンプソンは、負に帯電した「小体」が正電荷の均一な海に分布するモデルを提案しました。これはプラムプディングモデルとして知られています。
これらの小体は、1874年にイギリス系アイルランド人の物理学者であるジョージジョンストーンストーニーによって予測された理論上の粒子に基づいて、後で「電子」と名付けられました。そして、このことから、梅ケーキとレーズン。このコンセプトは、英国の1904年3月版で世界に紹介されました。 哲学雑誌、 絶賛する。
標準モデルの開発:
その後の実験により、プラムプディングモデルに多くの科学的な問題が明らかになりました。まず、原子が均一な正のバックグラウンド電荷を持っていることを示す問題があり、これは「トムソン問題」として知られるようになりました。 5年後、このモデルは、アルファ粒子と金箔(別名)を使用して一連の実験を行ったハンスガイガーとアーネストマースデンによって反証されます。 「金箔実験」。
この実験では、ガイガーとマースデンがアルファ粒子の散乱パターンを蛍光スクリーンで測定しました。トムソンのモデルが正しければ、アルファ粒子は妨げられることなく箔の原子構造を通過します。しかし、彼らは代わりに、ほとんどが真っ直ぐに撃たれたが、それらのいくつかは様々な方向に散らばっていて、いくつかは光源の方向に戻っていたと述べた。

ガイガーとマースデンは、トムソンのモデルで許容されるよりもはるかに大きな静電力が粒子に発生したと結論付けました。アルファ粒子はヘリウム原子核(正に帯電している)にすぎないため、これは原子の正の電荷が広く分散しておらず、小さな体積に集中していることを意味していました。さらに、偏向されなかった粒子が妨げられずに通過したという事実は、これらのポジティブスペースが空の巨大な湾によって隔てられていたことを意味します。
1911年までに、物理学者アーネストラザフォードはガイガーマースデン実験を解釈し、トムソンの原子モデルを拒否しました。代わりに、彼は、原子がほとんど空の空間で構成され、正の電荷がすべて電子雲に囲まれた非常に小さな体積の中心に集中するモデルを提案しました。これは、原子のラザフォードモデルとして知られるようになりました。
Antonius Van den BroekとNiels Bohrによるその後の実験により、モデルはさらに洗練されました。ヴァンデンブロークは元素の原子番号はその核電荷に非常に類似していると提案しましたが、後者は原子の太陽系のようなモデルを提案しました。核は正電荷の原子番号を含み、軌道殻の電子数(別名ボーア模型)。
電子雲モデル:
1920年代、オーストリアの物理学者アーウィンシュレディンガーは、マックスプランク、アルバートアインシュタイン、ニールスボーア、アーノルドゾンマーフェルト、その他の物理学者の理論に魅了されました。この間、彼は原子論とスペクトルの分野にも関与し、チューリッヒ大学で研究し、その後ベルリンのフリードリヒヴィルヘルム大学で研究を行いました(1927年にプランクの後任)。

1926年、シュレーディンガーは一連の論文で波動関数と電子の問題に取り組みました。シュレディンガー方程式と呼ばれることになるものを記述することに加えて、量子システムの量子状態が時間とともにどのように変化するかを記述する偏微分方程式-彼はまた、特定の位置で電子を見つける可能性を記述するために数式を使用しました。
これは、電子雲(または量子力学)モデルとして知られるようになるもの、およびシュレディンガー方程式の基礎となりました。すべての物質が波動関数に関連付けられたプロパティを持っていると述べる量子理論に基づいて、電子雲モデルは電子の正確な経路を定義しないという点でボーアモデルとは異なります。
代わりに、確率の関数に基づいて、電子の位置のありそうな位置を予測します。確率関数は基本的に、電子が見つかる可能性が高い雲のような領域を表すため、名前が付けられています。雲が最も密集している場所では、電子を見つける確率が最も高くなります。そして、電子の可能性が低い場所では、雲の密度は低くなります。
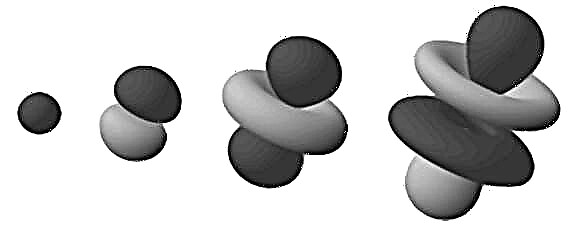
これらの高密度領域は、軌道を回る電子が見つかる可能性が最も高い場所であるため、「電子軌道」として知られています。この「クラウド」モデルを3次元空間に拡張すると、バーベルまたは花の形をした原子が表示されます(上の画像を参照)。ここで、分岐領域は、電子を見つける可能性が最も高い領域です。
シュレディンガーの研究のおかげで、科学者たちは量子力学の領域では電子の正確な位置と運動量を同時に知ることは不可能であることを理解し始めました。オブザーバーが粒子について最初に知っていることに関係なく、彼らは確率に関してその後続の位置または運動量のみを予測できます。
いずれの場合も、どちらかを確認することはできません。実際、彼らが粒子の運動量について知るほど、彼らはその位置について知ることが少なくなり、逆もまた同様です。これが今日「不確実性原理」として知られています。
前の段落で述べた軌道は、水素原子(つまり、電子が1つだけ)によって形成されることに注意してください。より多くの電子を持つ原子を扱う場合、電子軌道領域は球状のファジーボールに均一に広がります。これが「電子雲」という用語が最も適切な場所です。
この貢献は、20世紀のコスト重視の貢献の1つであると広く認識されており、物理学、量子力学、そして実際にすべての科学の分野で革命を引き起こしたものです。それ以来、科学者はもはや時間と空間の絶対的な性質を特徴とする宇宙ではなく、量子の不確実性と時間と空間の相対性で働いていました!
Space Magazineでは、原子と原子モデルについての興味深い記事を数多く書いています。ジョンダルトンの原子モデルとは何ですか、プラムプディングモデルとは何ですか、ボーアの原子モデルとは何ですか、誰がデモクリトスでしたか、そしてAtomのパーツは何ですか?
詳細については、「量子力学とは」を必ず確認してください。ライブサイエンスから。
天文学キャストは、エピソード130:ラジオ天文学、エピソード138:量子力学、およびエピソード252:ハイゼンベルクの不確定性原理のようなトピックに関するエピソードもあります。