19世紀後半、ロシアの化学者ドミトリメンデレーエフは、原子量に従って化学元素をグループ化するという彼の最初の試みを発表しました。当時知られている元素は約60個しかありませんでしたが、メンデレーエフは、元素を重量別に整理すると、特定の種類の元素が一定の間隔または周期で発生することに気付きました。
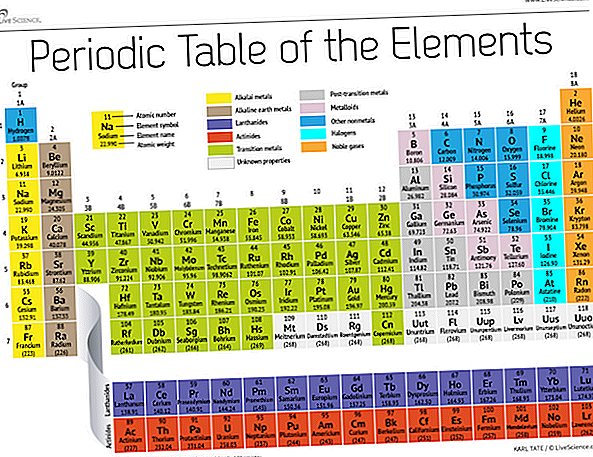
150年後の今日、化学者は118の元素を正式に認識し(2016年に4人の新人が追加された後)、メンデレーエフの元素周期表を使用してそれらを整理しています。この表は、最も単純な原子である水素から始まり、残りの元素を原子番号(各原子に含まれる陽子の数)で整理しています。少数の例外を除き、要素の順序は各原子の質量の増加に対応しています。
テーブルには7行と18列があります。各行は1つの期間を表します。元素の周期数は、その電子のエネルギーレベルの数を示します。たとえば、ナトリウムは3番目の期間にあります。つまり、ナトリウム原子は通常、最初の3つのエネルギーレベルに電子を持っています。表を下に移動すると、より大きく複雑な外部レベルを満たすためにより多くの電子が必要になるため、期間は長くなります。
テーブルの列は、要素のグループまたはファミリを表します。グループ内の要素は、最も外側のシェル(世界に表示される面)に同じ数の電子を持っているため、多くの場合、外観と動作は同じです。たとえば、テーブルの右端にあるグループ18の要素は、完全に完全な外殻を持ち、化学反応に参加することはほとんどありません。
元素は通常、金属または非金属のいずれかに分類されますが、2つの間の境界線はあいまいです。金属元素は通常、電気と熱の良導体です。金属内のサブグループは、これらのコレクションの同様の特性と化学的特性に基づいています。ロスアラモス国立研究所によると、周期表の説明では、一般に受け入れられている元素のグループを使用しています。
アルカリ金属: アルカリ金属は、表の最初の列であるグループ1の大部分を占めています。光沢があり、ナイフで切断できるほど柔らかく、これらの金属はリチウム(Li)で始まり、フランシウム(Fr)で終わります。また、非常に反応性が高く、水に触れると爆発したり爆発したりするため、化学者は油や不活性ガスに保管します。単一電子を持つ水素もグループ1に存在しますが、ガスは非金属と見なされます。
アルカリ土類金属: アルカリ土類金属は、ベリリウム(Be)からラジウム(Ra)までの周期表のグループ2を構成します。これらの元素のそれぞれは、最も外側のエネルギーレベルに2つの電子を持っています。これにより、アルカリ土類は十分に反応性になり、自然界で単独で見られることはほとんどありません。しかし、それらはアルカリ金属ほど反応しません。それらの化学反応は通常、アルカリ金属と比較してゆっくりと発生し、発熱が少なくなります。
ランタニド: 3番目のグループは長すぎて3番目の列に収まらないため、分割されて横に反転し、テーブルの下部に浮かぶ島の一番上の行になります。これは、元素57から71のランタニド、つまりランタン(La)からルテチウム(Lu)です。このグループの要素は銀白色で、空気に触れると変色します。
アクチニド: アクチニドは島の最下列に並び、89、アクチニウム(Ac)から103、ローレンシウム(Lr)の元素で構成されています。これらの元素のうち、トリウム(Th)とウラン(U)だけが地球上に大量に自然に発生します。すべてが放射性です。アクチニドとランタニドは一緒になって内部遷移金属と呼ばれるグループを形成します。
遷移金属: 表の本文に戻ると、グループ3〜12の残りの部分は残りの遷移金属を表しています。硬いが、順応性があり、光沢があり、導電性が高いため、これらの要素は、金属という言葉を聞いたとき、あなたが通常考えるものです。金、銀、鉄、プラチナなど、金属の世界で最もヒットしたものの多くがここに住んでいます。
遷移金属: 非金属の世界に飛び込む前に、共通の特徴は垂直のグループ線に沿ってきれいに分割されていません。遷移後の金属は、アルミニウム(Al)、ガリウム(Ga)、インジウム(In)、タリウム(Tl)、スズ(Sn)、鉛(Pb)、ビスマス(Bi)であり、グループ13からグループ17にまたがっています。これらの元素には、遷移金属の古典的な特性がいくつかありますが、他の遷移金属よりも柔らかく、伝導性が低い傾向があります。多くの周期表は、ホウ素とアスタチンを結ぶ対角線の下に太字の「階段」線を備えています。遷移後の金属はこの線の左下に集まっています。
メタロイド: メタロイドは、ホウ素(B)、シリコン(Si)、ゲルマニウム(Ge)、ヒ素(As)、アンチモン(Sb)、テルル(Te)、ポロニウム(Po)です。それらは金属から非金属への段階的な移行を表す階段を形成します。これらの元素は、導体としてではなく半導体(B、Si、Ge)として動作する場合があります。メタロイドは「セミメタル」または「貧金属」とも呼ばれます。
非金属: 階段の右上の他のすべて-水素(H)、グループ1に取り残された水素-は非金属です。これらには、炭素(C)、窒素(N)、リン(P)、酸素(O)、硫黄(S)、およびセレン(Se)が含まれます。
ハロゲン: フッ素(F)からアスタチン(At)までのグループ17の上位4つの元素は、非金属の2つのサブセットのうちの1つを表します。ハロゲンは化学的に非常に反応性が高く、アルカリ金属と対になってさまざまなタイプの塩を生成する傾向があります。たとえば、台所の食卓塩は、アルカリ金属ナトリウムとハロゲン塩素の結婚です。
希ガス: 無色、無臭、ほぼ完全に非反応性の不活性ガス、または希ガスがグループ18の表を完成させます。多くの化学者は、4つの新しく名前が付けられた要素の1つであるoganessonがこれらの特性を共有することを期待しています。ただし、この要素はミリ秒単位で測定される半減期を持っているため、直接テストすることはできませんでした。オガネッソンは周期表の7番目の期間を完了します。そのため、誰かが元素119を合成できた場合(そしてそのためのレースが既に進行中)、アルカリ金属カラムの行8を開始するためにループします。
テーブルに名前を付ける周期性によって作成される周期的な性質のため、一部の化学者はメンデレーエフのテーブルを円として視覚化することを好みます。
追加 資源: